Разработана новая модель оценки влияния ВИЧ и АРВТ на мозг

Несмотря на то, что многих негативных последствий ВИЧ-инфекции сегодня можно избежать, ситематически принимая антиретровирусную терапию (АРВТ), одной из областей, где медицинские исследования пока не достигли такого большого прогресса, является сфера когнитивных воздействий. Половина пациентов с ВИЧ имеют связанные с вирусом нейрокогнитивные расстройства (HAND), которые могут проявляться различными способами, от забывчивости и рассеянности до изменений поведения и двигательных нарушений.
Чтобы лучше понять механизмы, лежащие в основе HAND, исследователи из Школы стоматологии Пенна (Penn Dental Medicine) и Школы медицины им. Перельмана из Детской больницы Филадельфии (CHOP) в лабораторных условиях создали модель системы, использующей три типа клеток, которые принимают непосредственное участие в работе головного мозга, и проследили, какое влияние на них оказывают ВИЧ-инфекция и АРВТ.
«Честно говоря, у моделей, которые мы обычно используем в области ВИЧ, есть много недостатков, – говорит одна из авторов статьи, появившейся в журнале Stem Cell Reports, д-р Джордан-Скиутто. – Преимущество нашей модели заключается в том, что она позволяет нам взглянуть на взаимодействие между различными типами клеток человеческого мозга, а это куда более актуально для пациентов, чем что-либо иное».
В дополнение к исследованию ВИЧ члены команды рассчитывали также использовать эту модель, чтобы пролить свет на неврологические механизмы, лежащие в основе других состояний, таких как шизофрения, болезнь Альцгеймера и нормальное старение.
«Мы сотрудничаем с различными институтами, чтобы использовать эту систему для изучения болезни Альцгеймера, а также шизофрении, - говорит Стюарт Андерсон из CHOP и Penn Medicine. – У нас учтены все компоненты, которые, как мы знаем, взаимодействуют при этих заболеваниях, и это дает нам новый способ сочетания и подбора для объективной оценки того, как определенные клетки способствуют повреждению нейронов».
Действительно, толчок к созданию модели был дан не исследованиями о ВИЧ, а благодаря работе по шизофрении, которую д-р Шон Райан проводил в лаборатории Андерсона.
«Мы рассматривали роль микроглии, резидентных иммунных клеток центральной нервной системы, - говорит Райан. – Мы хотели понять, возможно ли проследить механистические изменения, которые происходят с микроглией при шизофрении».
Для этого Райану и Андерсону было интересно использовать индуцированные человеком плюрипотентные стволовые клетки – взрослые клетки, перепрограммированные в целях имитации эмбриональных стволовых клеток, – которые можно трансформировать в различные типы клеток.
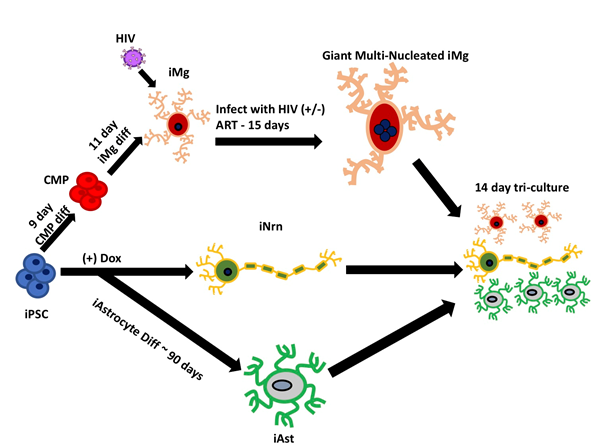
Заражая микроглию ВИЧ, а затем добавляя эти клетки к астроцитам и нейронам, команда обнаружила, что модельная система повторяет ключевые признаки повреждения, наблюдаемого в мозге во время ВИЧ-инфекции, с антиретровирусной терапией или без нее.
Однако шизофрения – это сложное заболевание с множеством сопутствующих генетических и внешних факторов, а также весьма широким спектром проявлений.
Вместо того, чтобы сразу наблюдать что-то сложное, ученые попытались применить свою новую модель к заболеванию, которое также наносит неврологический ущерб и где также участвует микроглия, - ВИЧ-инфекции.
Они обратились к д-ру Келли Джордан-Скиутто из Penn Dental Medicine, к тому времени имевшей большой опыт изучения механизмов HAND и желавшей разработать модель, превосходящую те, что были доступны ей прежде. Ученые совместно определили три типа клеток, которые их больше всего интересовали: нейроны, астроциты и микроглия.
Нейроны не поражаются ВИЧ напрямую, но известно, что они повреждаются во время инфицирования. Между тем, считается, что астроциты взаимодействуют с нейронами, имеющими повреждения, посылая провоспалительные сигналы в пространство между клетками, называемое синапсами. В то же время микроглия, которая отвечает за поддержание здоровой внешней среды при отсутствии заболеваний, в момент проникновения ВИЧ-инфекции расширяется и способствует воспалению.
После решения технической задачи по разработке новой модели, где каждый тип клеток генерировался независимо, а затем смешивался, команда использовала ее, чтобы установить, каким образом ВИЧ-инфекция и АРВТ влияют на клетки, как по отдельности, так и в комбинации.
«Многие люди принимают PreEP [доконтактную профилактику], когда они находятся в ситуации повышенного риска инфицирования ВИЧ, - говорит Райан. – Ввиду этого наравне с оценкой когнитивного воздействия ВИЧ нам также хотелось бы взглянуть, оказывают ли влияние эти препараты на состояние мозга здоровых людей».
Исследователи изучили экспрессию РНК в своих культурах, чтобы понять, какие именно белки и сигнальные процессы активируются в каждом сценарии. Во время инфекции они проследили возникновение воспалений, которые вызывались ими и были описаны в более ранних исследованиях. Когда же учеными был введен антиретровирусный препарат эфавиренз, активность большинства из них упала.
«Но в этом сценарии был свой уникальный ответ, – говорит Райан. – Некоторые процессы, связанные с воспалением и повреждением, остались, даже несмотря на введение препарата».
«Терапия EFZ в трех культурах, включающих ВИЧ-инфицированную микроглию, сокращает воспаление примерно на 70%, - говорит Райан. – Интересно, что EFZ сам по себе также вызывает воспаление, хотя и в меньшей степени, чем инфекция».
«Кажется, комбинация ВИЧ и АРВТ создает свой собственный уникальный ответ, который отличается от реакции каждой из частей системы в отдельности, - говорит Райан. – Знание того, какие процессы все еще активны благодаря АРВТ, может помочь нам соответствующим образом «направить» дополнительную терапию, чтобы у пациентов не развивались нейрокогнитивные расстройства».
Многие из особенностей инфекции, проявившихся в трехклеточной культуре, отразили то, что ученым уже было известно о ВИЧ-инфекции и АРВТ. Это дало им повод заявить, что их модель надежна.
«Просто взглянув на микроглию, - говорит Андерсон, - в нашей системе мы наблюдаем то, как она берет на себя свои обычные функции по поддержанию равновесия ключевых сигнальных систем как при нормальном состоянии, так и при активации и причинении вреда, когда организм борется с инфекцией. Теперь мы можем моделировать каждое из этих состояний».
По словам д-ра Джордан-Скиутто, новая модель «действительно изменит способ работы ее лаборатории в будущем». Она надеется, что многие другие ученые, работающие в области ВИЧ, продолжат их исследования, распространив их выводы на иные аспекты воздействия вируса на мозг.



